中国创新药的发展
中国创新药的发展
01 发展情况
生物制药行业始于19世纪末,至今已经历了四次浪潮,逐渐发展出以靶点为核心的研发道路。伴随着全球药企、研发机构、高校对于生物医药领域不停歇的探索,近些年创新药取得了许多重暗成果:首个完整无间隐的人类基因组序列测序的成功、CAR-T细胞疗法上市、人工智能辅助药物设计技术的应用、CRISPR/Cas9技术的使用等。不断涌现的新兴技术与靶点为全球创新药的发展注入新的活力,也意味着人类对于生物医药领域版图的持续拓展。
在全球创新药蓬勃发展的大环境下,中国药企也正在探索属于自己的创新药研发道路。过去20年,申国医药市场凭借医改推动和医保扩窑,从只占全球市场的2%一跃成为仅次于美国的全球第二大医药市场。从市场销售规模看,创新药仅占申国医院药物销售市场的25%。但随着仿制药一致性评价、带量采购等政策的开展,仿制药的发展空间越来越窄,发展创新药成为申国药企的重点。
然而,创新药的研发需要极高的研发能力以及巨额的供应资金,创新药的商业化亦需要丰富的专业知识以及强大的营销能力。长久以来,申国创新药既不具备有利的外部环境的支持,也不具有自我向上突破的实力与动力,行业发展曼限。自2016年《药品注册管理办法》修订后,申国创新药正式进入发展“快车道”。国家政府对于创新药的重视、资本对于创新药企业的关注推动申圄创新药的发展:申国创新药项目井喷式增妖、创新药研发政策不断规范、创新药市场日益扩大以及申国创新药企业在各个上市板块涌现。2020茸的新冠疫情爆发后,国产新冠疫苗的快速上市,无疑是申国创新药企业交上的一份令人满意的答卷,申国创新药已经起航。
近十年,为改变我国医药行业长久落后的现状,一系列政策不断出台,中国医药行业可谓发生了巨变,同时资本和人才也提供了巨大助力。由此,中国创新药行业发展环境迎来重大利好,行业发展处处焕发勃勃生机。
受制于时代发展水平的限制,过去我国对药物研发创新能力没有给予足够重视,医药相关政策也没有充分表现出鼓励创新的导向,仿制药往往是企业的第一选择。近些年政府发布了一系列对创新药利好的政策,以推动创新药企的发展。从临床、申报上市到落地使用的全流程,多种政策共同发力为中国创新药的快速发展营造出良好环境,为创新药发展奠定了基石。
医药行业的快速发展使得越来越多的资本关注到医药市场,一级市场表现活跃。二级市场也突破性地对上市规则进行改革,降低了对医药行业的上市要求,进一步推动了创新药行业欣欣向荣的局面。更多资本的流入为我国创新药的启动提供了充足的动力。
创新人才是创新药研发的内在核心,人才引进政策的推出为创新药发展做好了充分铺垫。近年来生物医药园区为引入优质人才,制定了优厚的人才引进政策,吸引一批又一批优质医药人才回国进行创业,为中国创新药行业注入新鲜血液。
02 政策促进
特殊审批管理条例
近年来,政府颁布和改革了多项政策以支持创新药的快速发展,其中包括特殊审批管理条例、先行区政策及医保政策。
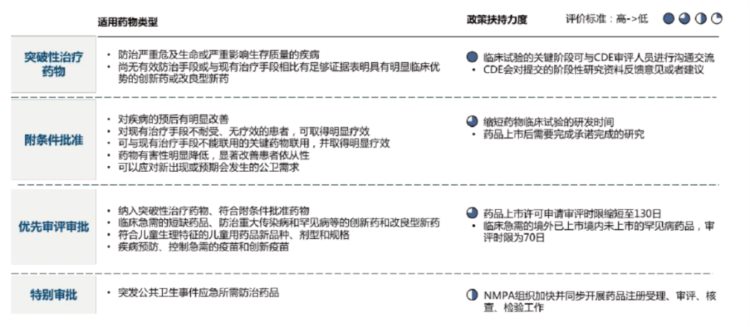
以鼓励药品创新,提升药品质量为导向,国家陆续出台了一系列针对新药注册的特殊审批管理规定,在加快新药注册步伐上取得了良好效果。2020年新修订的《药品注册管理办法》颁布,明确建立药品加快上市注册制度,支持以临床价值为导向的药物创新。《药品注册管理办法》设立了突破性治疗药物、附条件批准、优先审评审批、特别审批四个加快通道,并明确了每个通道的纳入范围、程序、支持政策等要求(如图1)。
图1 新药上市加速审评方式
先行区政策
建设先行区是我国对加速创新药行业发展的另一大政策创新模式,其能够通过临床使用国外已上市、国内未上市的药物,产生真实世界数据,达到加速药物上市的目的。2013年2月,海南博鳌国际医疗旅游先行区成立,允许临床急需的药品药械在指定医疗机构先行先试。
2015年大湾区概念提出,2019年2月大湾区发展规划纲要发布。海南博鳌乐城和大湾区的建立成功打造了与全球医疗资源高度协同接轨的特区。
截至目前,博鳌乐城和大湾区的先行政策已经助力多款药物临床使用及上市。2020年3月,我国首个使用境内真实世界数据的医疗器械产品艾尔建“青光眼引流管”获批上市,其在注册中使用了在海南博鳌乐城先行区收集的临床真实世界证据进行人种差异评价。2021年1月,强生全视Catalys飞秒激光眼科治疗系统基于博鳌乐城真实世界数据获批上市,成为继青光眼引流管之后第二例使用临床真实世界证据辅助临床评价获批的创新型医疗器械产品。
2021年3月,Blueprint Medicines普拉替尼胶囊成为首个真实世界数据辅助临床评价获批上市的药品。2021年4月,基于大湾区“港澳药械通”政策的落地实施,首个药品强生的“抗D免疫球蛋白注射液”和首个医疗器械“磁力可控延长铁棒”开始在深圳临床使用,这是第一款与香港特别行政区同步的新药。同月欧康维视OT-401的新药上市申请正式获NMPA受理,是首个完全基于先行区真实世界数据(博鳌乐城)申报的新药。
先行区能够助力多款药物临床使用及上市的原因在于先行区具有许多独特的福利政策。
以博鳌乐城为例,一是特许药械贸易自由便利,允许使用国际前沿、未在国内上市过的新药品、新器械。同时对于国外已上市国内未上市的临床急需特许药械,审批时间缩短至3个工作日。
二是开放真实数据应用研究,设立真实世界数据研究中,向国外已上市国内未上市的临床急需进口药械产品,在真实临床环境下使用产生数据,并支持药物在中国的获批上市。
三是将医疗和药品二合一监管,博鳌乐城创立了国内第一家由卫生部门和药监部门共同设立的医疗药品监管机构,使政府履行职能更加顺畅,实现业务协同、信息互通,资源共享,避免多头监管,形成监管合力,提高监管效率。从研发、临床试验、审批、上市使用等多个环节都为新药提供了极大的政策红利。
医保政策
除药品审批和先行区政策之外,国家对原有的医保政策也作出了大刀阔斧的改革,以适应和推动创新药的发展。
首先是对医保目录的调整时间进行了改革。以往医保目录调整时间间隔较长,不利于新药进入。国家医保局近年来逐渐建立起医保目录动态调整机制,原则上每年对医保目录调整一次。
其次是对医保目录的药品准入路径也进行了调整。伴随着国家谈判的发展进程,从2017年开始,谈判准入逐渐成为目录调整的重要方式。2019年医保目录调整方案明确规定我国医疗保障目录药品调整的准入路径分为常规准入和谈判准入两种。在满足有效性、安全性等前提下,价格(费用)与药品目录内现有品种相当或较低的,通过常规方式纳入目录;价格较高或对医保基金影响较大的专利独家药品应当通过谈判方式准入。近些年,谈判准入逐渐成为药品调入的主流。根据医药魔方
数据统计,2017年,国家医保目录通过常规准入的方式调入的药品数量还有339种,到2021年国家医保目录通过常规准入的方式调入的药品数量已经下降为7种,而通过谈判准入的方式调入的药品数量从2017年的44种上升为2021年的67种。随着医保制度的改革,创新药逐渐成为医保谈判的主流。
03 资本市场
根据医药魔方数据库统计已披露的投融资数据,2013年至2021年中国创新药领域在投资案例数量有了突破性的增长,在投资金额上也呈现出逐年上升的趋势。与2013年相比,2021年融资案例数增长超13倍,融资总金额超17倍(如图2)。
图2 2013-2021年中国创新药企业投融资情况
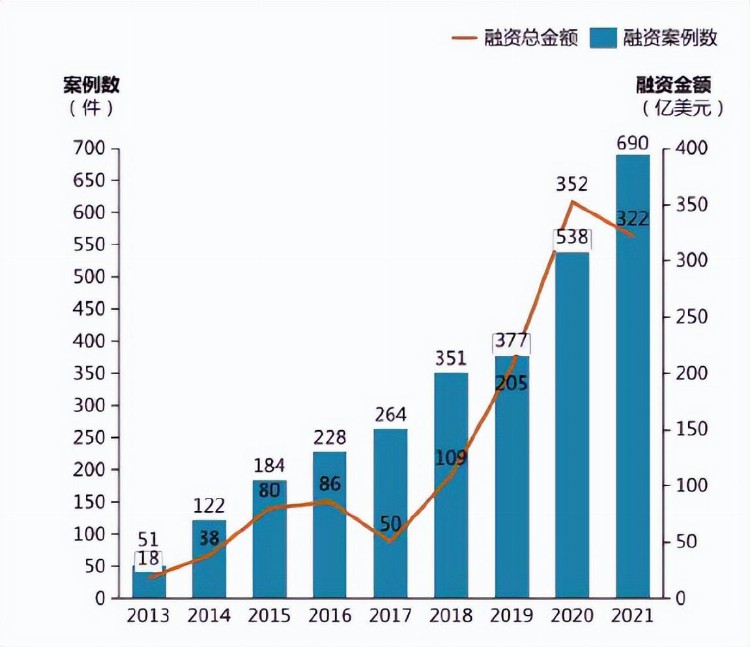
除了融资金额和融资数量的增长,一级市场的融资轮次也愈发早期。早期至A轮阶段的融资案例数由2013年的8件突破增长到2021年的252件,B轮融资也快速增长。资本对于创新药企业更加关注早期(如图3)。
图3 中国创新药企业融资热力图
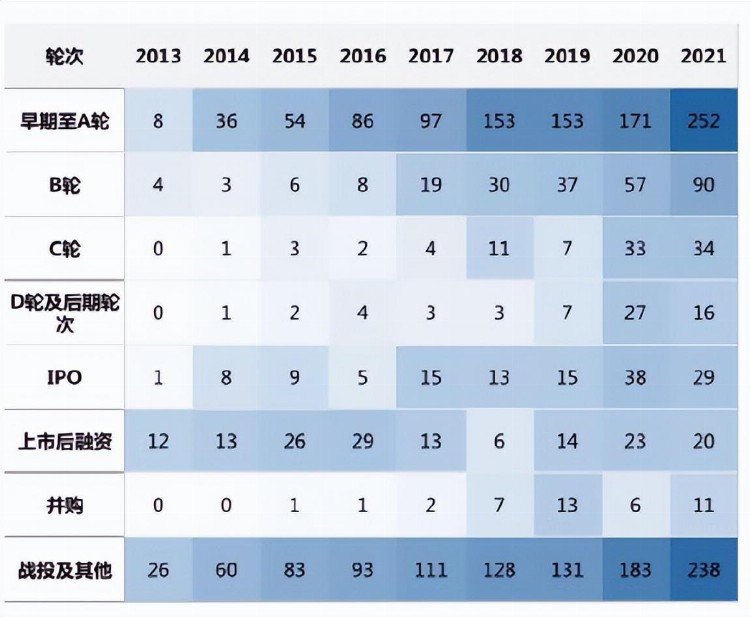
除一级市场表现活跃外,二级市场在交易所上市规则的改革与创新下也被大大激发活力,推动了医药企业的发展。
2018年4月30日,香港交易所新制订的《上市规则》生效,新规则规定接受同股不同权企业上市以及允许尚未盈利或者没有收入的生物科技公司赴港上市。港交所上市制度的改革给诸多拟上市企业提供了赴港上市的机会和可能。
2019年6月13日,上海证券交易所科创板正式开板,允许未盈利企业上市,其上市标准灵活,医药企业表现佳,产业链表现出细分子行业相对更丰富的特征。港股主板的改革和上交所科创板的创立,为生物医药公司的上市提供了有利支持,近些年涌现出一批在港股与科创板上市的创新药企业。据统计,2018-2021年共有75家企业通过港股及科创板上市,融资总金额达到257.5亿美元。
04 人才引进
创新药的研发需要资本的支持,也离不开具有研发能力的人才。创新人才是新药研发的驱动力。随着国家逐渐重视生物医药产业的发展,各地的生物医药产业园区、工业园区纷纷推出了生物医药行业人才的引进优惠政策,吸引人才,提供创业支持。
对于生物医药行业的高级人才,通常给予购房补贴、各种评审绿色通道、落户优惠、子女入学、社保医保优惠等政策吸引其入住园区。对于应届毕业生,在招聘、实习、落户等方面给予便利,设立生活补贴,吸引其加入园区企业。而在创业支持方面,园区通常会提供以下支持途径:一是设立相应计划,对于不同阶段项目的新药研发与转化提供资金支持;二是对认定的高新生物医药
企业提供生产、研发用地的建设支持等,帮助初创企业更好地建设公司;三是为初创企业提供投融资帮助,对于投资机构设立奖励等方式,吸引投资机构投资园区内部。
以苏州工业园区举例,出台了《关于加快集聚生物医药产业人才的若干措施》共15条全方面的措施。其中例如,措施规定对于生物医药人才开通绿色通道,优先享受园区人才优购房、人才优租房和虚拟优租房政策;支持生物医药重点企业引进硕士、博士应届毕业生人才,给予硕士每年3万元、博士每年4万元,累计不超过3年的人才补贴;对于入选科技领军人才创新创业工程的生物医药人才提供创新创业资助,最高补贴资助可达5000万元且顶尖人才补贴金额上不封顶。
受益于政策、资本、人才等多因素共振,中国创新药企业蓬勃发展,在市场和研发端都有较好表现。在市场端,上市创新药数量明显增长,其中国产创新药数量大副曾多,且在药品销售中,随着上市创新药数量的增多,中国医药市场创新药销售占比不断提高,同时国产创新药也逐渐进入市场,份额逐年增长。在研发端,中国创新药企业创新能力显著增强,近五年来不仅在创新IND和NDA数量上升,同时FIC能力也有了快速发展,并且中国创新药企业研发能力也逐步被国外企业认可,License out项目逐年增长,还出现了大金额交易事件。
END


